细胞铁死亡(Ferroptosis):是一种铁依赖性脂质过氧化物的积累所导致新型细胞死亡的方式。主要是由铁超载和活性氧(ROS)依赖的脂质过氧化物累积引起的。线粒体是铁利用、分解代谢和合成代谢途径的主要细胞器,细胞发生铁死亡时线粒体与正常线粒体相比膜密度更致密,体积更小,嵴减少或消失,外膜破裂等。
1. 铁死亡相关特征
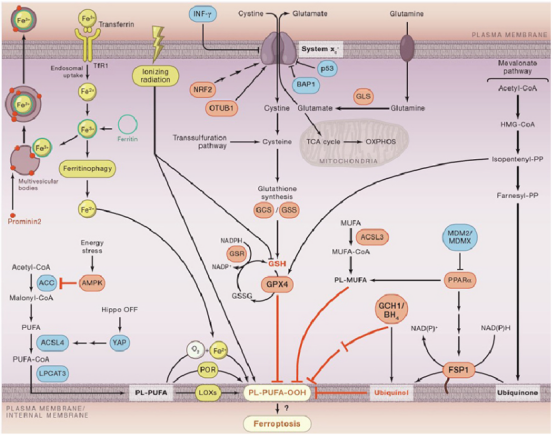
铁死亡的的本质是谷胱甘肽的耗竭,谷胱甘肽过氧化物酶(GPX4)活性下降,脂质氧化物不能通过GPX4催化的谷胱甘肽还原酶反应代谢,之后二价的铁离子氧化脂质产生活性氧,从而促使铁死亡的发生。
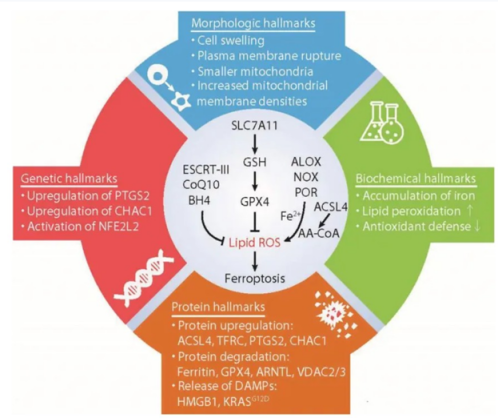
铁死亡在细胞形态学特征、生化特征以及基因水平特征上都与凋亡、自噬、坏死等传统的细胞死亡方式具有显著的变化,具体表现为:
1)细胞形态学特征
超微形态学特征显示细胞膜断裂,线粒体变小、膜密度增高、线粒体脊减少或消失、线粒体外膜断裂,细胞核大小正常、但缺乏染色质凝聚。电镜下表现为细胞内线粒体变小及双层膜密度增高。
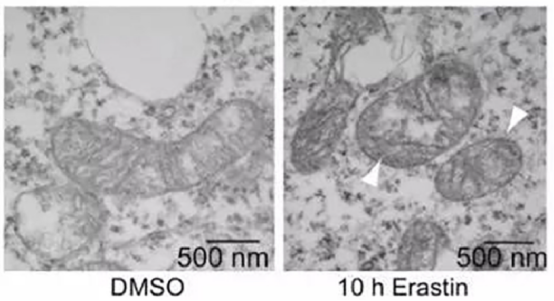
2)生化特征变化
铁和活性氧(ROS)聚集,激活丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)系统,降低胱氨酸的摄取、耗竭胞内谷胱甘肽(GSH),抑制胱氨酸/谷氨酸反向转运蛋白system Xc- 和增加NADPH氧化酶(NOXs),释放花生四烯酸(ARA)等介质。
3)基因水平特征变化
铁死亡受细胞内信号通路的严密调节,包括铁稳态的调节通路,RAS/Raf/MAPK通路以及胱氨酸转运通路。
细胞内Cox2, ACSL4, NOX1, GPX4, SLC7A11, Ferritin和Ferritin Light Chain等相关因子发生变化,其中Cox2, ACSL4和NOX1在铁死亡细胞中表达上调; GPX4, SLC7A11, Ferritin和Ferritin Light Chain在铁死亡细胞中表达下调。
4)免疫学特征
损伤相关分子模式(damage-associated molecular patterns,DAMPs)释放前炎症介质(如HMGB1等)。
2. 铁死亡常见检测方法
1)形态学观察
细胞形态观察:利用透射电镜直接对细胞形态进行观察,细胞发生铁死亡时线粒体变小以及线粒体膜密度较大;
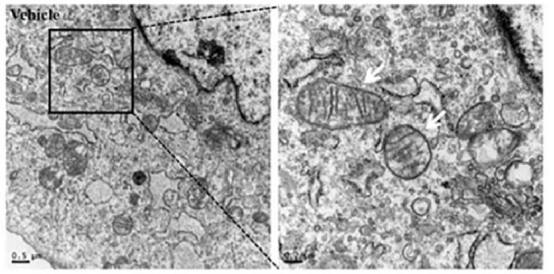
线粒体形态观察:向细胞内转染LifeAct-GFP荧光蛋白,一定时间后通过有丝分裂追踪器观察线粒体的形态。

2)新陈代谢检测
①细胞活性检测 CCK-8:可用于简便而准确的细胞增殖和毒性分析。
②细胞内铁水平检测:可以使用PGSK探针检测,通过流式细胞术或共聚焦显微镜监测活细胞内铁含量的细胞膜透性染料,在铁死亡的细胞中,PGSK的绿色荧光会减弱。
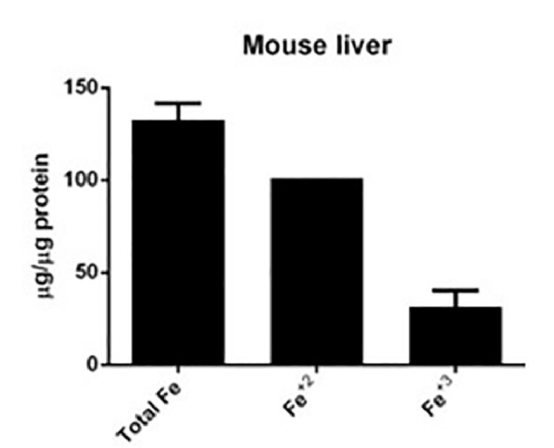
3)活性氧水平检测
通过C11-BODIPY探针检测,在铁死亡细胞中,探针会由红色转化为绿色。
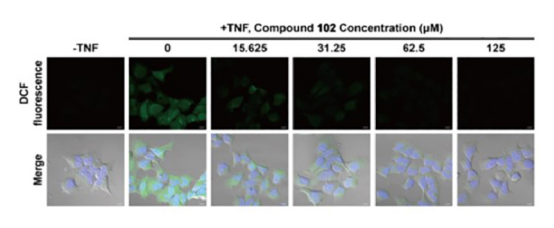
4)线粒体膜电位检测
可以使用TMRE荧光染料检测,TMRE能够特异性标记有活性的线粒体,是一种细胞膜可穿透性的,正电荷的,橘红色荧光染料。当线粒体膜电位降低时,荧光减弱。
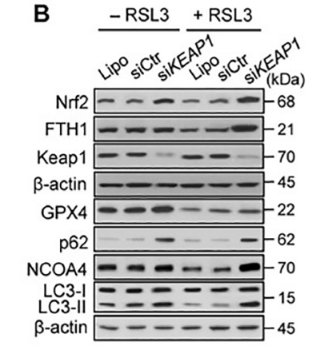
2)qPCR/Western Blot检测
检测细胞内与铁死亡相关的因子变化,例如Cox2, ACSL4和NOX1在铁死亡细胞中表达上调; GPX4, SLC7A11, Ferritin和Ferritin Light Chain在铁死亡细胞中表达下调。